

深圳湾实验室/粤港澳大湾区国际临床试验中心及北京大学深圳研究生院的Andrew Stephen Lee博士,斯坦福大学医学院的Patricia K. Nguyen 博士,中国医学学院阜外医院的兰峰博士,和苏州大学附属第一医院及心血管科学研究所的沈振亚教授作为共同通讯作者;第一作者为北京大学深圳研究生院的博士研究生尤祎和田雨,以上研究人员于2025年1月20日在《欧洲心脏杂志(European Heart Journal)(IF:38,心血管医学领域排名第一)发表了这一研究成果,标志着心血管病基因治疗迈入了一个崭新的时代。
缺血性损伤是包括美国和中国在内的世界上导致死亡和疾病的第一大原因,血管内皮生长因子(VEGF)基因治疗为缺血性损伤患者带来了希望。然而,传统的病毒载体(如腺相关病毒AAV)的高免疫原性和脂质纳米颗粒(LNP)的低表达效率一直是VEGF递送的瓶颈,导致以往的多项临床试验失败。最近,一种基于工程化细胞工程化外囊泡(Extracellular vesicle, EV)的新型基因疗法被证明能够解决AAV和LNP的障碍:与携带VEGF基因装载物的AAV和LNP相比,装载血管内皮生长因子A(VEGF-A)信使RNA(mRNA)的细胞工程化外囊泡表现出较低的免疫原性和有效的递送能力。
突破瓶颈:VEGF-A细胞工程化外囊泡提供了一种病变组织基因递送的新方式
在基因治疗探索的过程中,如何高效、安全地将治疗基因传递到靶组织一直是研究人员面临的巨大挑战。传统的递送方法,如腺相关病毒(AAV)和脂质纳米颗粒(LNP),已经实现了核酸(如DNA和mRNA)的递送,但其固有的免疫原性会限制治疗效果,甚至可能引发严重的免疫反应,不仅破坏基因治疗装载物,而且还会对接受这些治疗的患者产生副作用。
为了突破这一瓶颈,该研究团队独辟蹊径,将目光投向了工程化外囊泡这一天然的纳米级递送载体。工程化外囊泡作为细胞分泌的一种微小囊泡,具有卓越的生物相容性和低免疫原性,能够轻松跨越多种生物屏障,将携带的遗传物质精准递送到目标细胞。研究团队前期开发了第一个皮肤病学mRNA治疗方法—细胞外囊泡(EV)递送mRNA的胶原蛋白替代疗法(You Y et al., Nat Biomed Eng 2023), 延续性研究中又成功地将全长血管内皮生长因子A(VEGF-A)mRNA包裹在成纤维细胞来源的工程化外囊泡中,制备出了高mRNA含量的VEGF-A工程化外囊泡。这一创新性的递送方式,不仅实现了VEGF-A mRNA的高效递送,更显著降低了免疫原性,为基因治疗领域带来了一种全新的解决方案。
血管新生:VEGF-A工程化工程化外囊泡促进组织修复与再生
在缺血性血管疾病的治疗中,血管新生扮演着至关重要的角色,旨在恢复组织的血液灌注并改善其功能。VEGF-A(血管内皮生长因子-A)作为一种至关重要的血管生长因子,在诱导血管新生方面展现出了显著的效果。它能够有力地促进血管内皮细胞的增殖和迁移,为新生血管的形成奠定基础。
然而,传统的VEGF-A蛋白注射或基因治疗方法存在明显的局限性,如半衰期短暂、靶向性不足等,这极大地限制了其在实际应用中的疗效。
本研究开创性地提出了利用VEGF-A工程化外囊泡进行治疗的新思路。通过将外源性的VEGF-A mRNA递送到缺血组织,研究团队显著地提升了VEGF-A蛋白的表达水平。在股动脉或冠状动脉结扎后给予人VEGF-A工程化外囊泡的小鼠模型中,研究团队观察到血管新生的现象明显增强。这些新生血管不仅在数量上有所增加,而且在结构上也更加成熟,有效地改善了缺血组织的血液灌注状况。同时,VEGF-A工程化外囊泡还展现出了促进左心室功能恢复的潜力,为缺血性心脏病的治疗开辟了新的途径。
低免疫原性:VEGF-A工程化工程化外囊泡引领基因治疗新模式
在基因治疗过程中,免疫原性是一个不容忽视的问题。传统的AAV和LNP递送方式往往引发强烈的免疫反应,导致治疗效果受限。相比之下,VEGF-A工程化外囊泡凭借其天然的低免疫原性特性,在注射部位和全身范围内均未引发显著的先天性或适应性免疫反应。
本研究通过比较VEGF-A AAV、VEGF-A LNP和VEGF-A工程化外囊泡三种不同递送方式在小鼠模型中的免疫反应发现,VEGF-A AAV会引发强烈的先天性和适应性免疫反应,而VEGF-A LNP则主要引发强烈的先天性免疫反应和低度的适应性免疫反应。相比之下,VEGF-A工程化外囊泡的递送仅引起低度的先天性免疫反应和低度的适应性免疫反应,表现出极高的安全性和耐受性。这一发现不仅为VEGF-A工程化外囊泡在基因治疗中的应用提供了有力的证据,也为其他基因治疗载体的设计和优化提供了新的思路。
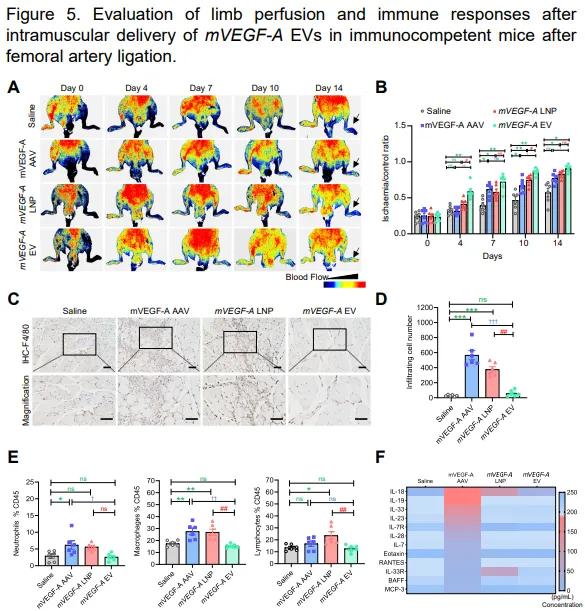
图:术后肢体灌注及免疫活性评价mVEGF-A EV在股动脉结扎术后小鼠肌内递送:与生理盐水对照组(右侧股动脉结扎)相比,mVEGF-A AAV、mVEGF-A LNP和mVEGF-A EV mRNA均有助于肢体缺血血运重建。然而,mVEGF-A EV mRNA的血运重建速度更快,可能是由于C-F图中所示的免疫原性较低。
重复给药:VEGF-A工程化工程化外囊泡展现了持久治疗效果
在疾病的治疗过程中,重复给药是一种常见的策略,其目的在于通过增加药物暴露的时间和剂量来增强治疗效果。然而,这种做法也可能带来潜在的风险,例如在AAV介导的基因治疗中,重复给药会带来免疫原性的增强和毒性反应的加剧。因此,开发一种既能有效增强治疗效果,又能避免上述风险的新型给药方式显得尤为重要。本研究针对这一挑战,探讨了VEGF-A工程化外囊泡在受伤皮肤中的序贯递送效果。结果显示,这种给药方式不仅能够显著改善伤口愈合效果,而且未观察到明显的免疫反应或毒性反应。
这表明,与常规药物相比,VEGF-A工程化外囊泡在单次给药时即表现出高效性和安全性。更重要的是,在重复给药过程中,VEGF-A工程化外囊泡仍能保持稳定的治疗效果,同时展现出低免疫原性的特性。这一发现为VEGF-A工程化外囊泡在慢性缺血性血管疾病和需要长期治疗的疾病中的应用提供了广阔的前景。随着科技的进步和研究的深入,基因治疗正逐渐成为治疗多种疾病的重要手段。然而,传统的递送方式所面临的免疫原性和靶向性问题一直是制约其发展的关键因素。本研究通过创新性地利用工程化外囊泡作为递送载体,成功制备了高效、低免疫原性的VEGF-A工程化外囊泡细胞工程化外囊泡疗法,为心脏病、中风、肢体缺血等缺血性血管疾病的治疗带来了新的希望。未来,随着研究的不断深入和技术的不断完善,相信这种新型基因疗法将进入临床试验,并显示出其独特的优势和潜在的其他治疗适应症。
文章来源 | Andrew S. Lee课题组
参考文献:
1、Yi You, Yu Tian, Rui Guo, Junfeng Shi, Kwang Joo Kwak, Yuhao Tong, Andreanne Poppy Estania, Wei-Hsiang Hsu, Yutong Liu, Shijun Hu, Jianhong Cao, Liqun Yang, Rui Bai, Pufeng Huang, Ly James Lee, Wen Jiang, Betty Y S Kim, Shuhong Ma, Xujie Liu, Zhenya Shen, Feng Lan, Patricia Kim Phuong Nguyen, Andrew S Lee. Extracellular vesicle-mediated VEGF-A mRNA delivery rescues ischaemic injury with low immunogenicity. Eur Heart J. 2025 Jan 20:ehae883. doi: 10.1093/eurheartj/ehae883.
2、You Y#, Tian Y#, Yang Z#, Shi J, Kwak KJ, Tong Y, Estania AP, Cao J, Hsu WH, Liu Y, Chiang CL, Schrank BR, Huntoon K, Lee D, Li Z, Zhao Y, Zhang H, Gallup TD, Ha J, Dong S, Li X, Wang Y, Lu WJ, Bahrani E, Lee LJ, Teng L, Jiang W, Lan F*, Kim BYS*, Lee AS*. Intradermally delivered mRNA-encapsulating extracellular vesicles for collagen-replacement therapy. Nat Biomed Eng. 2023 Jul;7(7):887-900. doi: 10.1038/s41551-022-00989-w. Epub 2023 Jan 12. PMID: 36635419.